Практическая работа 3 ГДЗ Габриелян 10 класс (углубленный уровень) (Химия)
Решение #1



Рассмотрим вариант решения задания из учебника Габриелян Остроумов Пономарев 10 класс, Дрофа:
Практическая работа №3
Спирты
Растворимость спиртов в воде
В отдельные пробирки прилейте по 1 — 2 мл этилового и изоамилового (изопентилового) спиртов. Добавьте к ним по 2—3 мл воды и взболтайте. Отметьте, что этиловый спирт полностью растворился в воде, а изоами-ловый спирт отделяется при отстаивании в виде маслянистого слоя над водой.
Вопросы
1. В чём причина различного поведения спиртов в воде?
Этанол – молекула содержит небольшой по размерам этильный радикал и высокополярную гидрокси-группу, поэтому он хорошо растворяется в полярных растворителях, например, воде. Хорошей растворимости в воде также способствует образование водородной связи.
Изоамиловый спирт вместе с полярной гидрокси-группой содержит относительно большой и разветвленный углеводородный радикал. Это неполярный фрагмент молекулы, который ухудшает растворимость вещества в воде, однако способствует высокой растворимости в неполярных органических растворителях (например, в гексане)
2. Почему изоамиловый спирт отслаивается над водой, а не наоборот?
При расслаивании несмешивающихся друг с другом жидкостей, верхний слой занимает вещество с меньшей плотностью. Плотность изоамилового спирта 0,8 г/мл, воды – 1 г/мл, поэтому спирт сверху.
3. Какие жидкие органические вещества при смешивании с водой будут образовывать слой над водой?
Чтобы расслаиваться над водой, органическое вещество не должно в ней растворяться и должно иметь меньшую плотность. Этим условиям удовлетворяют: толуол (0,87 г/мл), бензол (0,71 г/мл).
Вывод: по мере роста молекулярной массы растворимость спиртов в воде уменьшается, что демонстрируется высокой растворимостью этанола и низкой растворимостью изоамилового спирта.
Окисление этилового спирта оксидом меди (II)
На конце медной проволоки сделайте 5—6 витков спирали (можно обернуть её вокруг авторучки или карандаша). В пробирку налейте 5 мл этилового спирта. Накалите медную спираль в пламени спиртовки, чтобы медь покрылась чёрным налётом оксида, а затем быстро опустите её в пробирку со спиртом. Напишите уравнение протекающей реакции.
Данную операцию повторите десять раз. Обратите внимание на появление запаха образующегося ацеталь-дегида и на изменения, происходящие со спиралью.
Вопросы
1. Протекает ли данная реакция при комнатной температуре?
При комнатной температуре реакция не идет, необходимо нагревание.
2. Возможно ли дальнейшее окисление уксусного альдегида оксидом меди (II) до уксусной кислоты?
Даже при 10-кратном повторении не появляется запаха уксуса (что свидетельствовало бы о выделении уксусной кислоты), поэтому дальнейшее окисление невозможно
Вывод: при нагревании оксид меди (II) окисляет этанол до ацетальдегида.
Окисление этилового спирта дихроматом калия
В пробирке смешайте 2 мл 5%-го раствора дихромата калия и 1 мл 20% -го раствора серной кислоты. Отметьте цвет раствора. Добавьте к окислительной смеси 0,5 мл этилового спирта. Отметьте изменение цвета раствора. Почувствуйте появление характерного запаха образующегося уксусного альдегида.
Вопросы
1. Почему изменяется цвет окислительной смеси после добавления этилового спирта? Напишите уравнение протекающей реакции.
2. Можно ли заменить серную кислоту в данной реакции на соляную?
Дихромат калия – очень сильный окислитель, который может окислить не только спирт, но и другие вещества в смеси. В серной кислоте сера в максимальной степени окисления, поэтому она не может быть окислена. В соляной кислоте, наоборот, хлор в составе хлорида, можно окислить до чистого хлора. Поэтому заменять серную кислоту на соляную не следует.
3. Окисляются ли в аналогичных условиях третичные спирты?
В третичных спиртах не возможно окисление ни до альдегида, ни до кетона.
Вывод: дихромат калия в кислой среде окисляет этанол до ацетальдегида, о чем свидетельствует изменение окраски раствора.
Получение глицерата меди
В пробирку налейте около 1 мл 10%-го раствора сульфата меди (II) и добавьте немного 10%-го раствора гидроксида натрия до образования голубого осадка гидроксида меди (II).
К полученному осадку добавьте по каплям глицерин. Взболтайте смесь. Отметьте превращение голубого осадка в раствор тёмно-синего цвета.
Вопросы
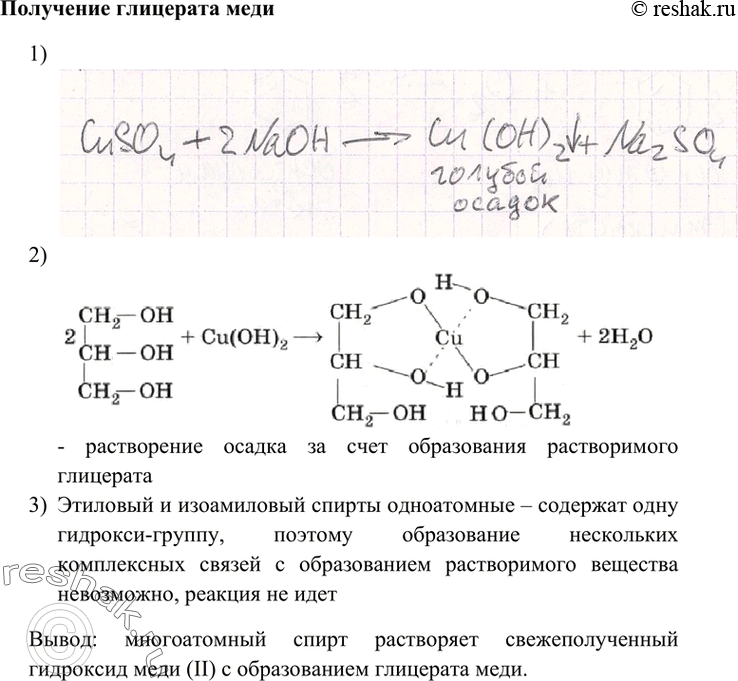
1. Какая реакция лежит в основе получения гидроксида меди (II)? Напишите уравнение этой реакции.
2. Почему при добавлении глицерина к осадку гидроксида меди (II) осадок растворяется? С чем связано интенсивное окрашивание раствора? Напишите уравнение реакции глицерина с гидроксидом меди (II).
3. Будут ли этиловый и изоамиловый спирты реагировать с гидроксидом меди (II)?
Этиловый и изоамиловый спирты одноатомные – содержат одну гидрокси-группу, поэтому образование нескольких комплексных связей с образованием растворимого вещества невозможно, реакция не идет
Вывод: многоатомный спирт растворяет свежеполученный гидроксид меди (II) с образованием глицерата меди.
Похожие решебники
Популярные решебники 10 класс Все решебники
*размещая тексты в комментариях ниже, вы автоматически соглашаетесь с пользовательским соглашением







