Часть II Параграф 30 ГДЗ Рабочая тетрадь Габриелян 9 класс (Химия)
Решение #1


Рассмотрим вариант решения задания из учебника Габриелян, Сладков 9 класс, Дрофа:
Часть II
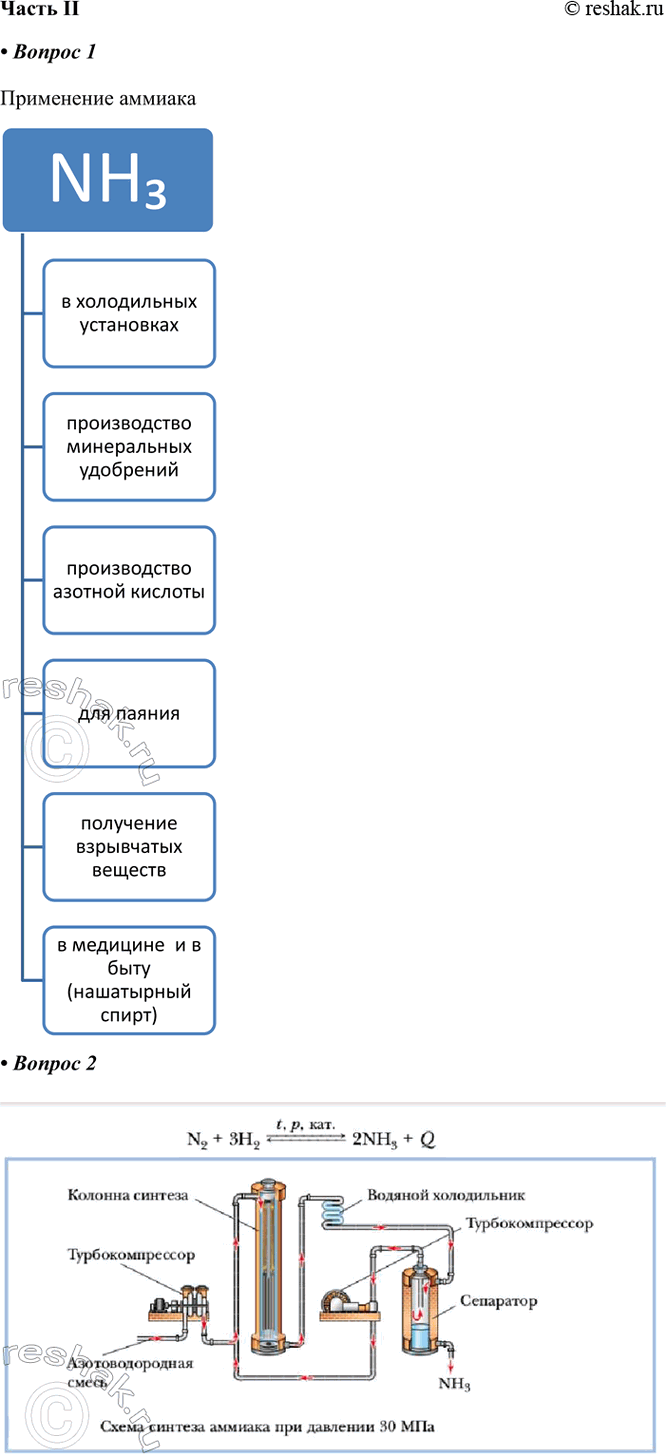
1. Заполните схему «Применение аммиака».
2*. Зарисуйте схему промышленного синтеза аммиака, укажите сырьё и происходящие процессы.
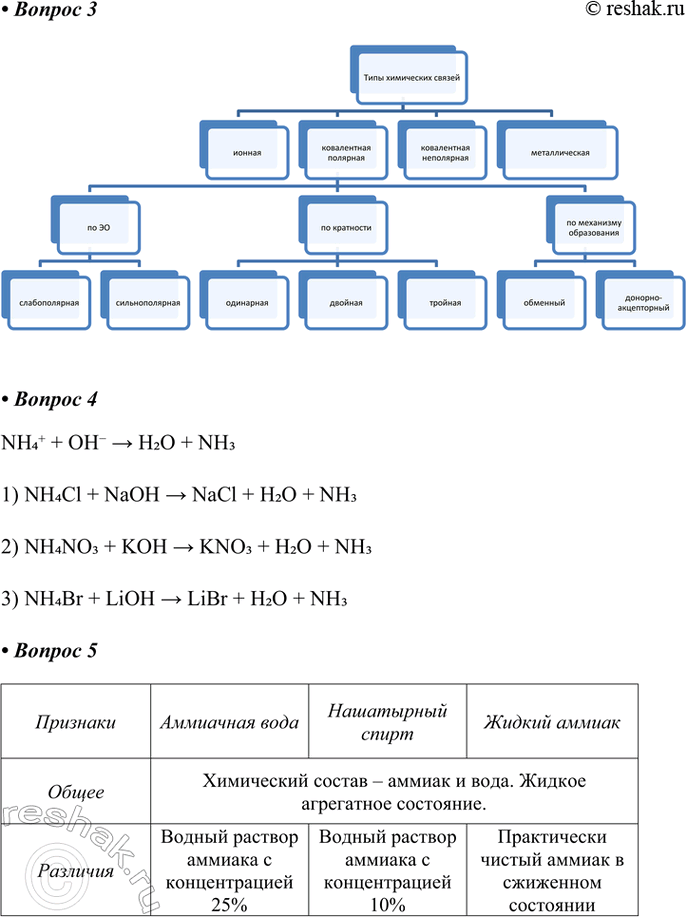
3. Заполните схему «Типы химических связей».
4. Предложите три молекулярных уравнения, отражающих качественную реакцию на ион аммония:
NH4+ + OH- > H2O + NH3
1) NH4Cl + NaOH > NaCl + H2O + NH3
2) NH4NO3 + KOH > KNO3 + H2O + NH3
3) NH4Br + LiOH > LiBr + H2O + NH3
5. Заполните таблицу.
ПРИЗНАКИ — АММИАЧНАЯ ВОДА — НАШАТЫРНЫЙ СПИРТ — ЖИДКИЙ АММИАК
Общее
Химический состав – аммиак и вода. Жидкое агрегатное состояние.
Различия
Водный раствор аммиака с концентрацией 25%
Водный раствор аммиака с концентрацией 10%
Практически чистый аммиак в сжиженном состоянии
6. Какой объём аммиака образуется при взаимодействии 535 г 20%-го раствора хлорида аммония с щёлочью?
Дано:
m(раствора NH4Cl)=535 г
w(NH4Cl)=20%
M(NH4Cl)= 53,5 г/моль
Vm= 22,4 л/моль
V(NH3)=?
NH4Cl + KOH > KCl + H2O + NH3^
m(NH4Cl)= m(раствора NH4Cl) · w(NH4Cl) / 100% = 535·0,2= 107 (г)
n(NH4Cl)=m/M=107/ 53,5 =2 (моль)
x=n(NH3)= 2·1/1=2 (моль)
V(NH3)=n· Vm=2 ·22,4= 44,8 (л)
Ответ. 44,8 л.
7. Запишите уравнения реакций для следующих переходов.
1) N2 + 3H2 > 2NH3
2) NH3 + HCl > NH4Cl
3) NH4Cl + KOH > NH3^ + KCl + H2O
4) NH3 + HNO3 > NH4NO3
5) NH4NO3 + KOH > NH3^ + KNO3 + H2O
6) 4NH3 + 3O2 > 2N2 + 6H2O
Похожие решебники
Популярные решебники 9 класс Все решебники
*К сожалению, временные проблемы с публикацией комментариев с мобильных устройств.









