Страница 137 ГДЗ Рабочая тетрадь Габриелян 8 класс (Химия)
Рассмотрим вариант решения задания из учебникаГабриелян 8 класс, Дрофа:
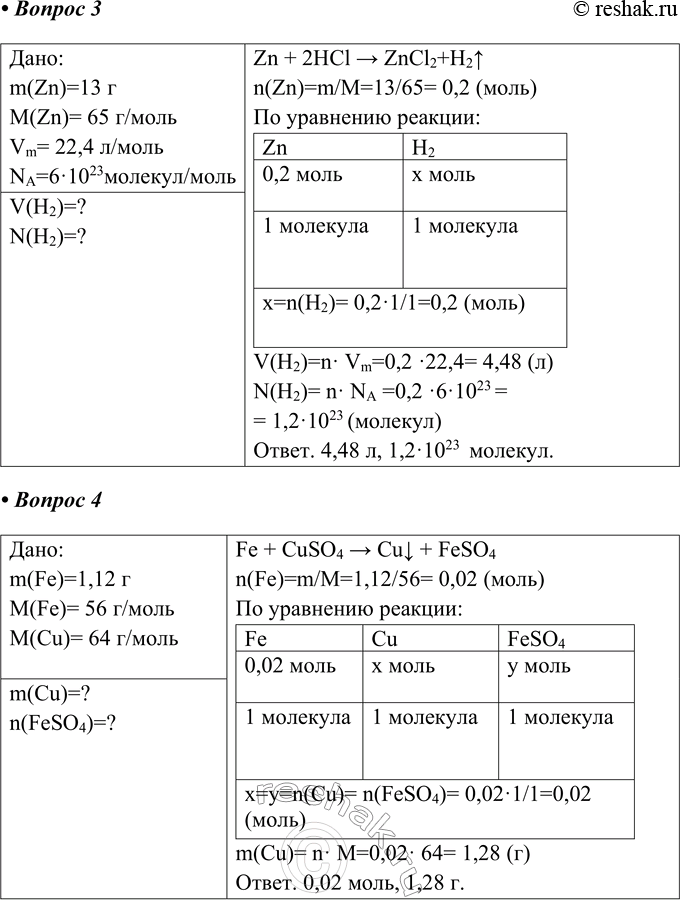
3. В реакцию вступили 13 г пинка и соляная кислота. В результате реакции образовались водород и хлорид цинка. Определите объём (н. у.) и число молекул водорода.
1) Запишите уравнение реакции (коэффициенты!)
2) Рассчитайте количество вещества цинка
3) Рассчитайте количество водорода
4) Рассчитайте объём водорода
5) Вычислите число молекул водорода
Дано:
m(Zn)=13 г
M(Zn)= 65 г/моль
Vm= 22,4 л/моль
NA=6·1023молекул/моль
Zn + 2HCl > ZnCl2+H2^
n(Zn)=m/M=13/65= 0,2 (моль)
По уравнению реакции:
Zn H2
0,2 моль x моль
1 молекула 1 молекула
x=n(H2)= 0,2·1/1=0,2 (моль)
V(H2)=n· Vm=0,2 ·22,4= 4,48 (л)
N(H2)= n· NA =0,2 ·6·1023 = = 1,2·1023 (молекул)
Ответ. 4,48 л, 1,2·1023 молекул.
4. Навеска 1,12 г железа полностью «растворилась» в растворе сульфата меди (II). Вычислите массу образовавшегося осадка меди. Какое количество вещества сульфата железа (II) получилось при этом?
Дано:
m(Fe)=1,12 г
M(Fe)= 56 г/моль
M(Cu)= 64 г/моль
Fe + CuSO4 > Cuv + FeSO4
n(Fe)=m/M=1,12/56= 0,02 (моль)
По уравнению реакции:
Fe Cu FeSO4
0,02 моль x моль y моль
1 молекула 1 молекула 1 молекула
x=y=n(Cu)= n(FeSO4)= 0,02·1/1=0,02 (моль)
m(Cu)= n· M=0,02· 64= 1,28 (г)
Ответ. 0,02 моль, 1,28 г.
Похожие решебники
Популярные решебники 8 класс Все решебники
*К сожалению, временные проблемы с публикацией комментариев с мобильных устройств.








