Параграф 38 ГДЗ Кузнецова Титова 8 класс (Химия)

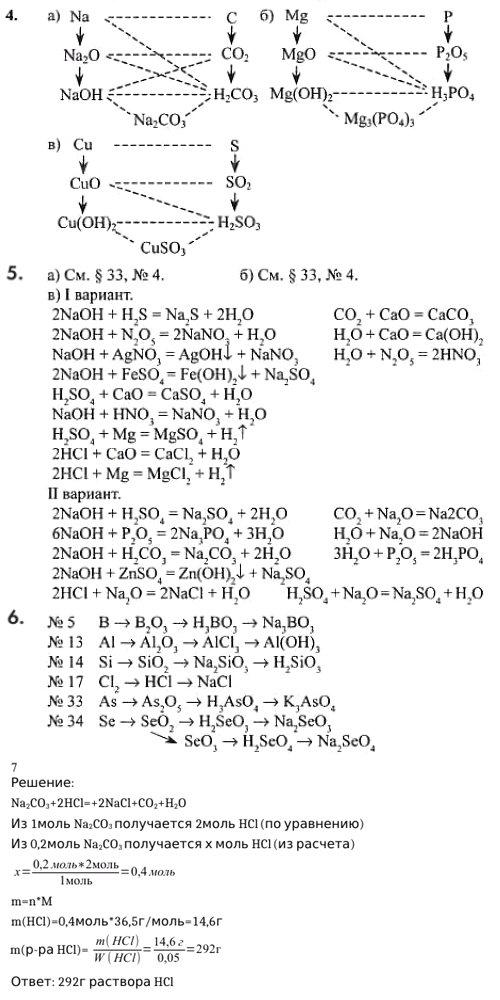
Рассмотрим вариант решения задания из учебника Кузнецова, Титова 8 класс, Просвещение:
1. Составьте уравнения реакций, раскрывающие следующие превращения:
Cu — CuО — Cu(NO3)2 — Cu(ОН)2 — CuО — CuSO4
2Cu + O2 = 2CuO
CuO + 2HNO3 = Cu(NO3)2 + H2O
Cu(NO3)2 + 2NaOH = Cu(OH)2v + 2NaNO3
Cu(OH)2 = CuO + H2O
CuO + H2SO4 = CuSO4 + H2O
2. С какими из перечисленных веществ вступит в реакции раствор гидроксида кальция (известковая вода): хлорид цинка, железо, оксид серы (IV), сульфат меди (II), нитрат свинца(II), оксид железа (II), бромоводородная кислота?
Ca(OH)2 + ZnCl2 = Zn(OH)2v + CaCl2
Ca(OH)2 + SO2 = CaSO3 + H2O
Ca(OH)2 + CuSO4 = Cu(OH)2v + CaSO4
Ca(OH)2 + Pb(NO3)2 = Pb(OH)2v + Ca(NO3)2
Ca(OH)2 + 2HBr = CaBr2 + 2H2O
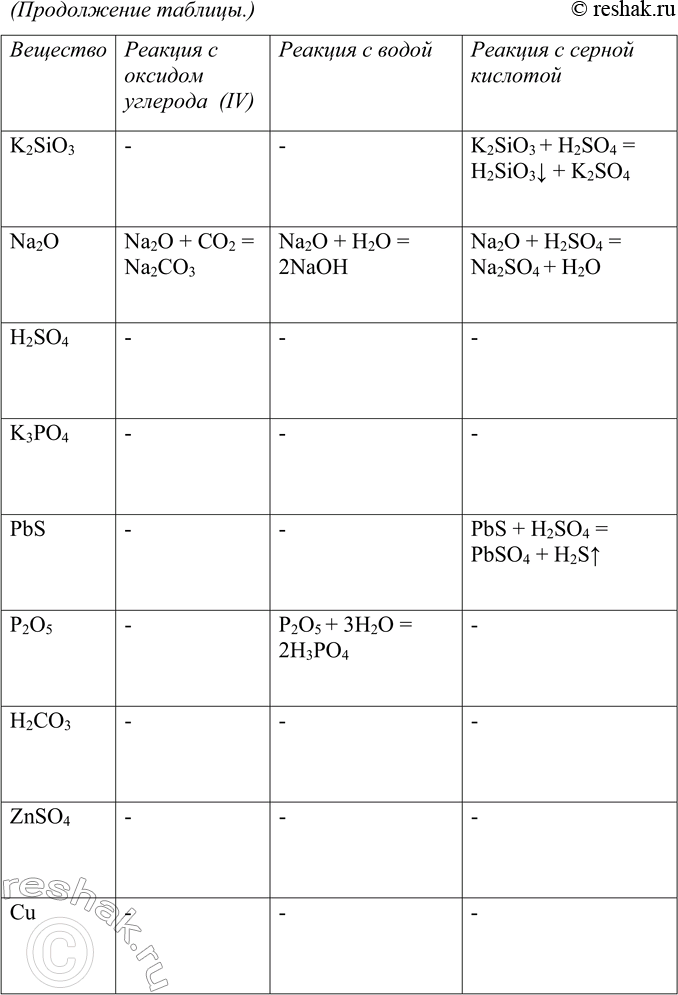
3. Из веществ, формулы которых даны в варианте H малого химического тренажёра (табл. 20, с. 144), выберите те, что будут вступать в реакцию со следующими химическими соединениями: а) оксид кальция; б) гидроксид железа (II); в) баритовая вода; г) нитрат свинца (H).
А) С оксидом кальция реагируют:
H2SO4 + CaO = CaSO4 + H2O
P2O5 + 3CaO = Ca3(PO4)2
H2CO3 + CaO = CaCO3 + H2O
Б) С гидроксидом железа (II) реагирует:
H2SO4 + Fe(OH)2 =FeSO4 + 2H2O
В) С баритовой водой реагируют:
H2SO4 + Ba(OH)2 =BaSO4v + 2H2O
3Ba(OH)2 + 2K3PO4 = Ba3(PO4)2v + 6KOH
P2O5 + 3Ba(OH)2 = Ba3(PO4)2v + 3H2O
H2CO3 + Ba(OH)2 = BaCO3v + 2H2O
ZnSO4 + Ba(OH)2 = BaSO4v + Zn(OH)2v
Г) С нитратом свинца (II) реагируют:
K2SiO3 + Pb(NO3)2 = 2KNO3 + PbSiO3v
H2SO4 + Pb(NO3)2 = PbSO4v + 2HNO3
2K3PO4 + 3Pb(NO3)2 = Pb3(PO4)2v + 6KNO3
H2CO3 + Pb(NO3)2 = PbCO3v + 2HNO3
ZnSO4 + Pb(NO3)2 = PbSO4v + Zn(NO3)2
4. Пользуясь составленными схемами, напишите уравнения реакций, возможных между веществами, представленными на рисунке 71.
Пусть M – Ca, тогда:
2Ca + O2 = 2CaO
CaO + H2O = Ca(OH)2
Пусть Нм – P, тогда:
4P + 5O2 = 2P2O5
P2O5 + 3H2O = 2H3PO4
3Ca + 2P = Ca3P2
3Ca + 2H3PO4 = Ca3(PO4)2 + 3H2^
3CaO + P2O5 = Ca3(PO4)2
3CaO +2H3PO4 = Ca3(PO4)2 + 3H2O
3Ca(OH)2 + P2O5 = Ca3(PO4)2 + 3H2O
3Ca(OH)2+2H3PO4 = Ca3(PO4)2 + 6H2O
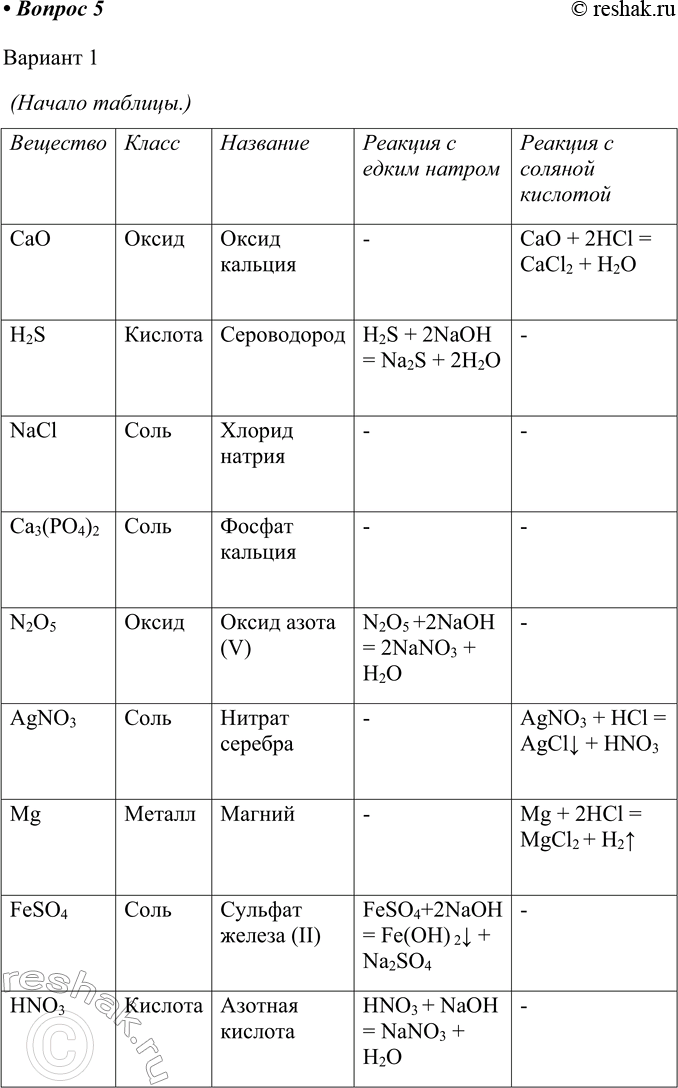
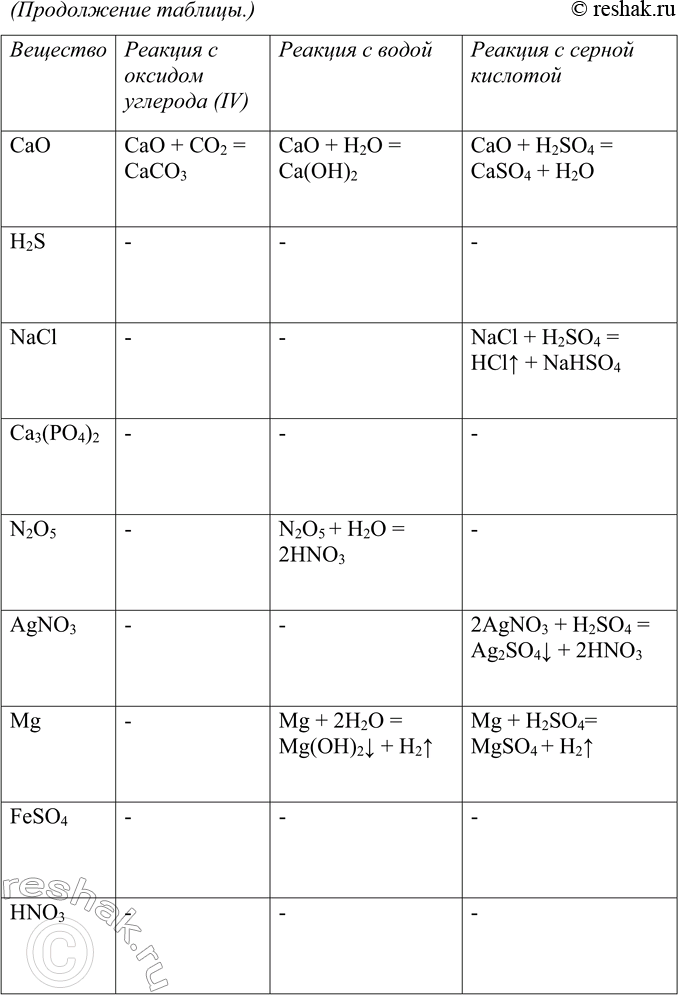
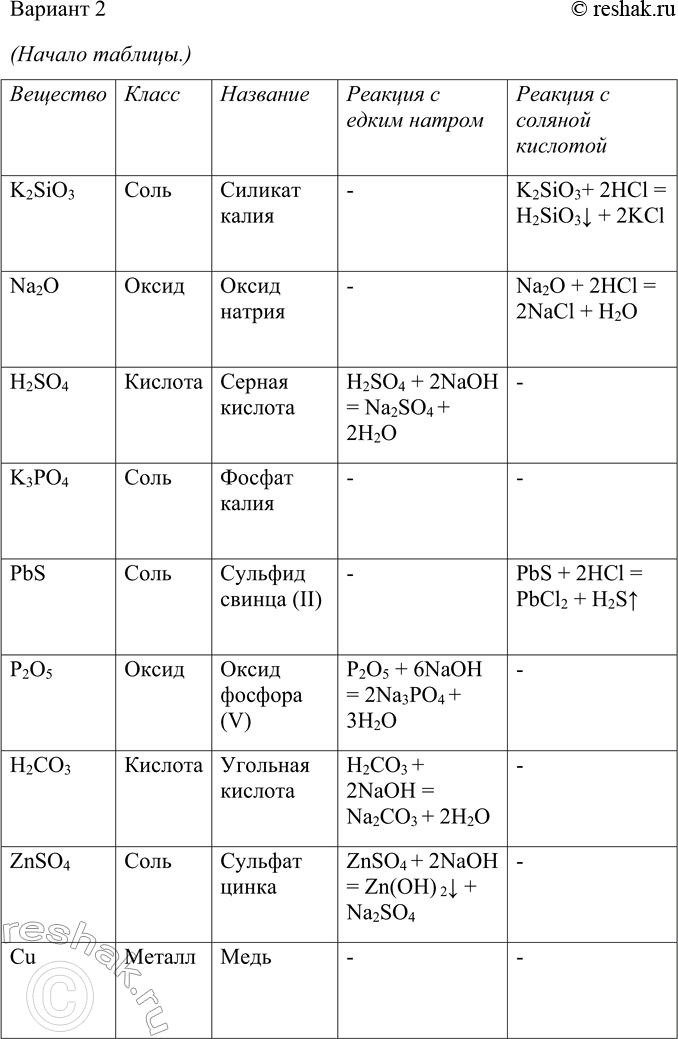
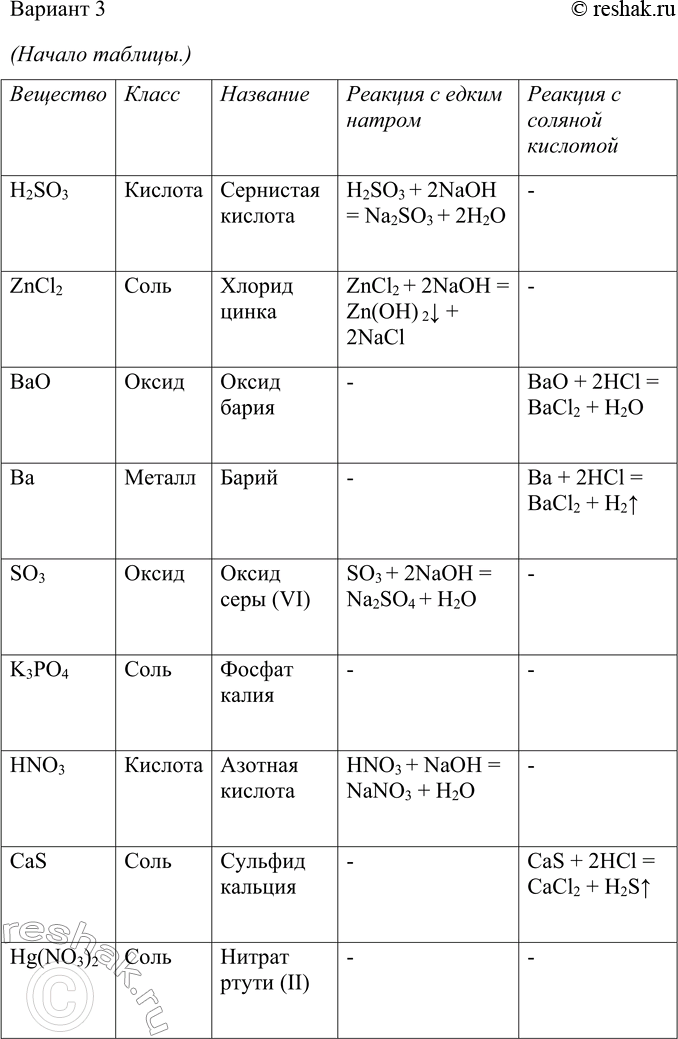
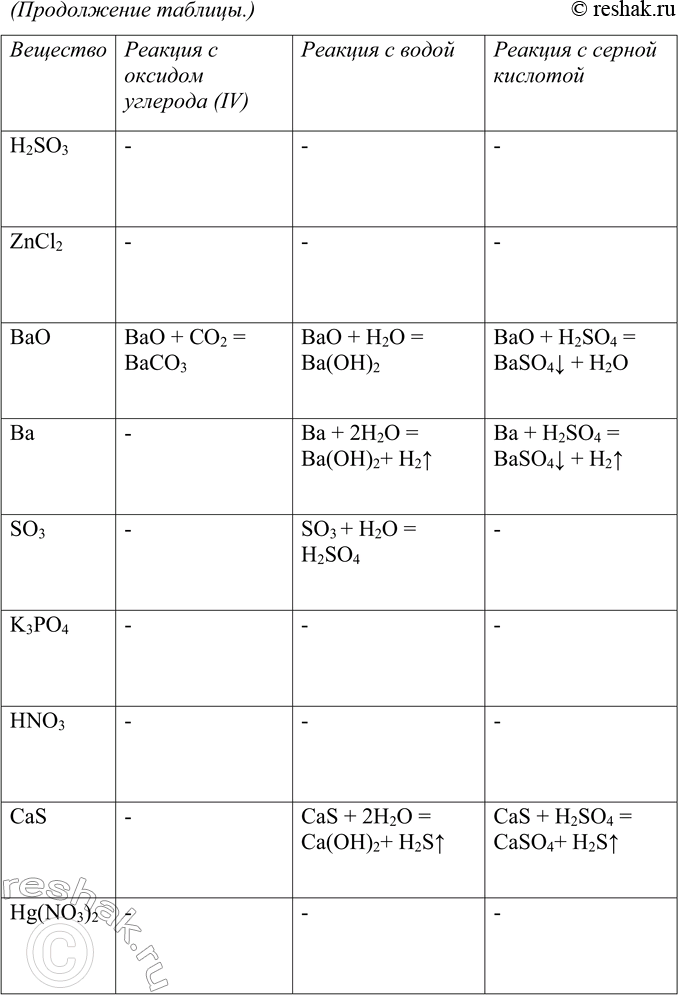
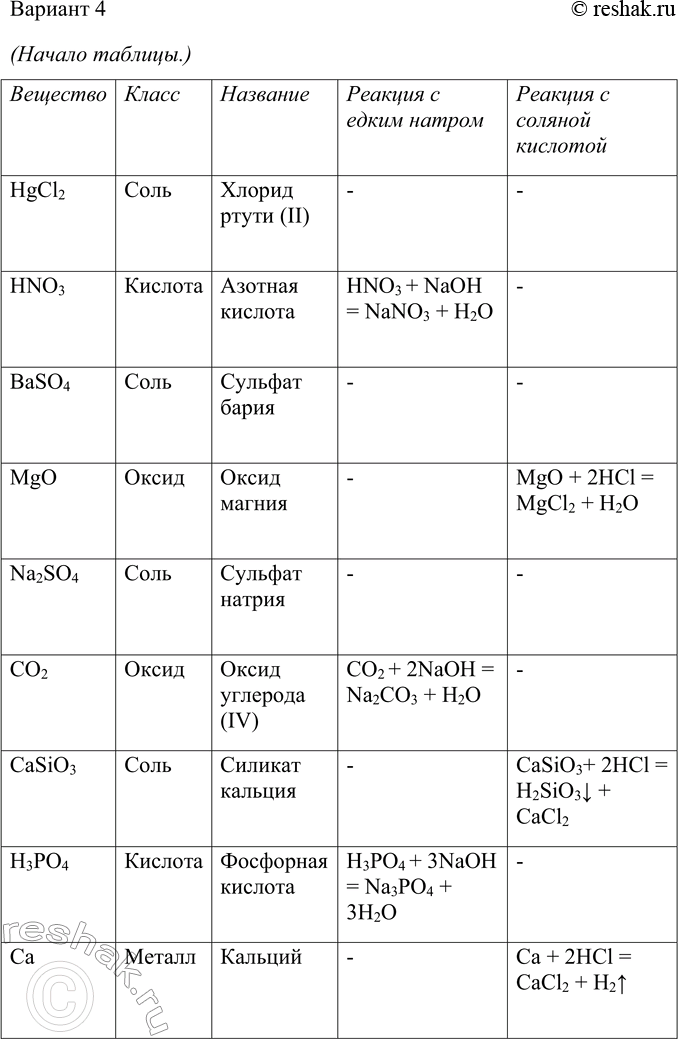
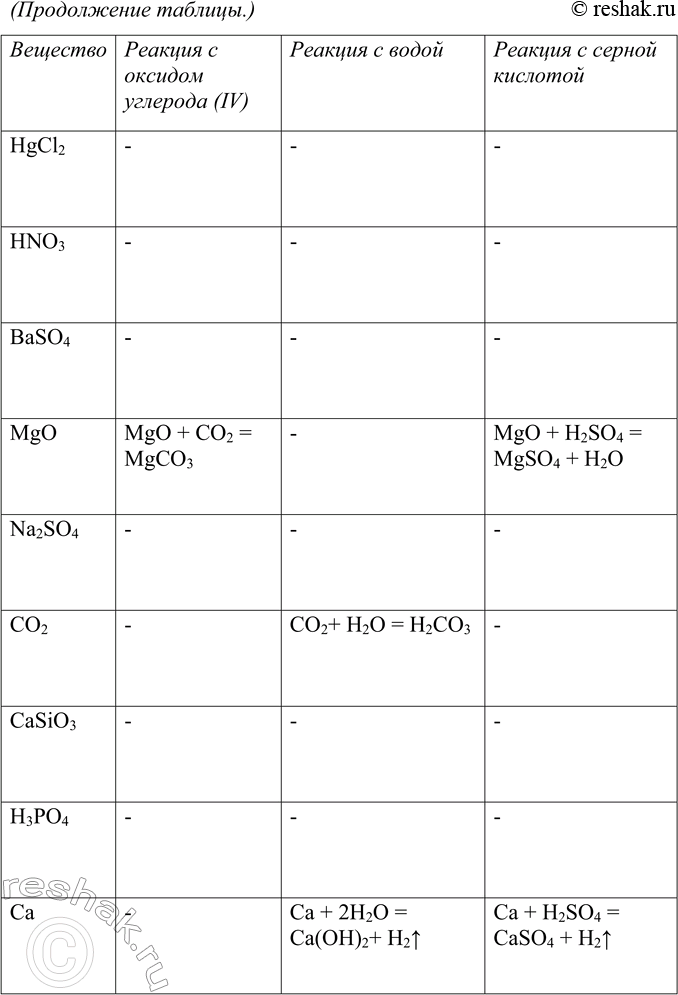
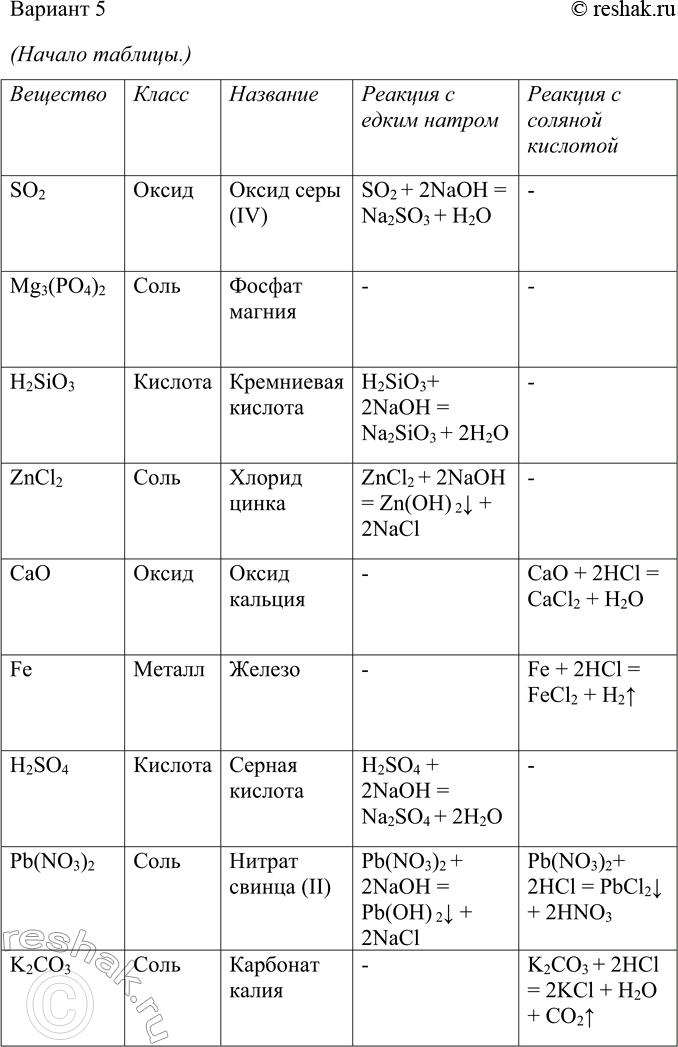
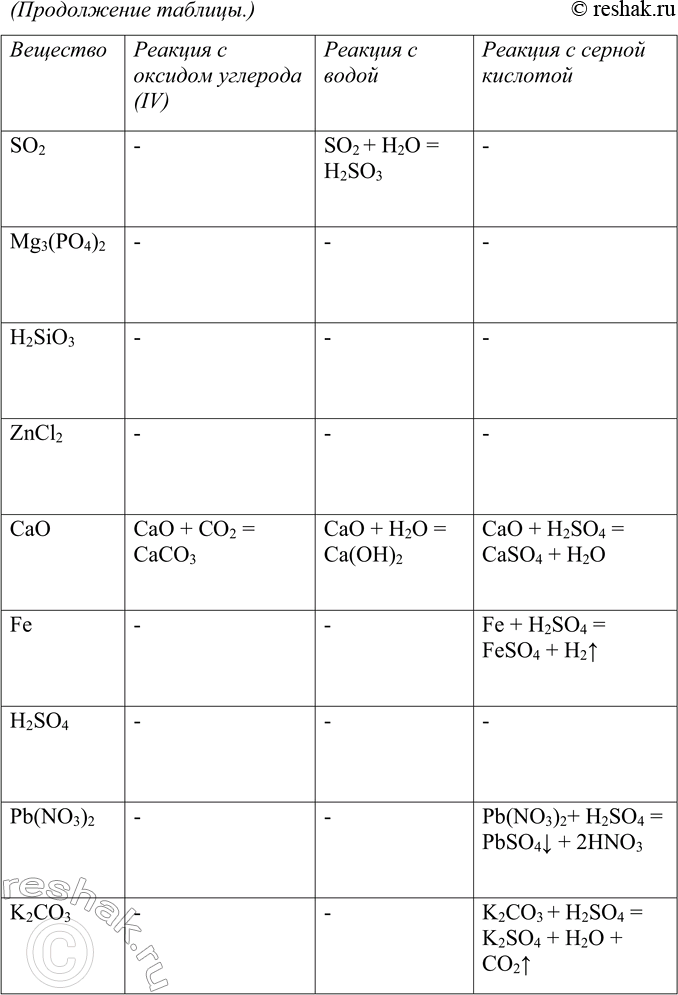
5. Пользуясь малым химическим тренажёром (табл. 20, с. 144) (учитель укажет вам номер варианта), выполните следующие задания:
а) дайте названия веществам, формулы которых приведены в вашем варианте;
б) укажите принадлежность каждого вещества к определённому
классу. На основании каких признаков состава вы классифицировали каждое вещество?
в) составьте уравнения возможных химических реакций между веществами вашего варианта и едким натром, соляной кислотой, оксидом углерода (IV), водой, серной кислотой.
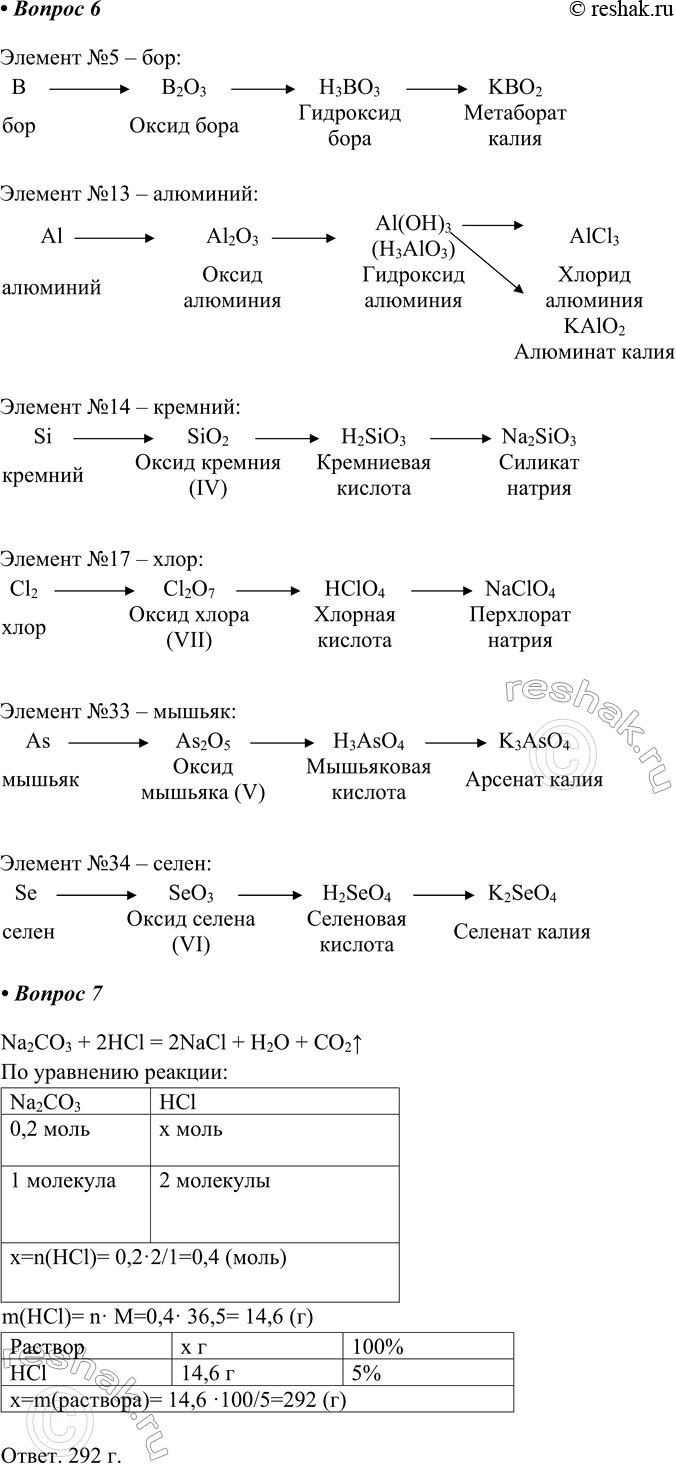
6. Составьте схемы генетической связи соединений, образованных атомами элементов № 5, 13, 14, 17, 33, 34 в периодической таблице.
7. Для проведения химической реакции с 0,2 моль карбоната натрия использовали раствор, массовая доля хлороводорода в котором 5 %. Определите массу взятого раствора.
Na2CO3 + 2HCl = 2NaCl + H2O + CO2^
m(HCl)= n· M=0,4· 36,5= 14,6 (г)
Ответ. 292 г.
Популярные решебники 8 класс Все решебники
*К сожалению, временные проблемы с публикацией комментариев с мобильных устройств.





