Тема 19 Часть 1 ГДЗ Рабочая тетрадь Габриелян 11 класс (Химия)


Рассмотрим вариант решения задания из учебника Габриелян, Сладков 11 класс, Просвещение:
§ Роль воды в химических реакциях
Часть I
• Вопрос 1
Заполните схему.
• Вопрос 2
Электролиты – это вещества, которые в растворах распадаются на ионы – диссоциируют.
Признаки электролитов: состоят из ИОНОВ; растворяются в ВОДЕ
• Вопрос 3
Диссоциация – это распад электролита на ионы в растворе.
• Вопрос 4
Основные положения ТЭД
1. По способности проводить электрический ток в растворах все вещества делятся на
Электролиты
1) Щелочи: NaOH, KOH, Ca(OH)2
2) Растворимые кислоты: HCl, H2SO4, HNO3
3) Растворимые соли: NaCl, KNO3, CuSO4
Неэлектролиты
1) Нерастворимые основания: Fe(OH)3, Al(OH)3
2) Нерастворимая КИСЛОТА: H2SiO3
3) НЕРАСТВОРИМЫЕ соли: BaSO4, AgCl
4) Оксиды
5) Почти все органические
вещества
6) Простые вещества
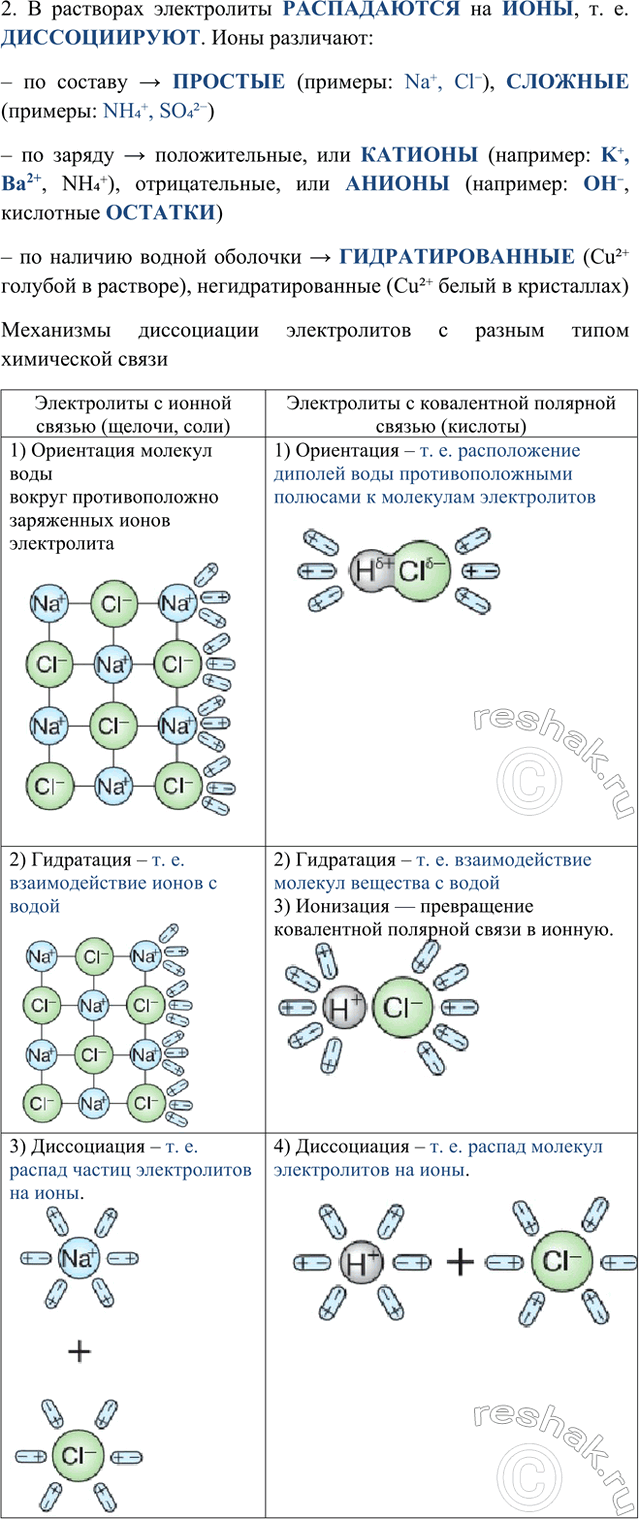
2. В растворах электролиты РАСПАДАЮТСЯ на ИОНЫ, т. е. ДИССОЦИИРУЮТ. Ионы различают:
– по составу > ПРОСТЫЕ (примеры: Na+, Cl-), СЛОЖНЫЕ (примеры: NH4+, SO42-)
– по заряду > положительные, или КАТИОНЫ (например: K+, Ba2+, NH4+), отрицательные, или АНИОНЫ (например: OH-, кислотные ОСТАТКИ)
– по наличию водной оболочки > ГИДРАТИРОВАННЫЕ (Cu2+ голубой в растворе), негидратированные (Cu2+ белый в кристаллах)
Механизмы диссоциации электролитов с разным типом химической связи
Электролиты с ионной связью (щелочи, соли)
1) Ориентация молекул воды
вокруг противоположно
заряженных ионов электролита
2) Гидратация – т. е. взаимодействие ионов с водой
3) Диссоциация – т. е. распад частиц электролитов на ионы.
Электролиты с ковалентной полярной связью (кислоты)
1) Ориентация – т. е. расположение диполей воды противоположными полюсами к молекулам электролитов
2) Гидратация – т. е. взаимодействие молекул вещества с водой
3) Ионизация — превращение ковалентной полярной связи в ионную.
4) Диссоциация – т. е. распад молекул электролитов на ионы.
3. Разные электролиты по-разному диссоциируют на ионы, что характеризует степень электролитической диссоциации – а
а зависит:
• от природы электролита: чем более полярна молекула вещества, тем больше а
• от разбавления: чем выше степень разбавления, тем больше а
Как электролиты, все вещества делятся на три класса.
1) Кислоты – это электролиты, которые диссоциируют на КАТИОНЫ ВОДОРОДА и АНИОНЫ КИСЛОТНОГО ОСТАТКА
Например: HNO3 = H+ + NO3-
H2SO4 = 2H+ + SO42-
2) Основания – это электролиты, которые диссоциируют на катионы металла и гидроксид-анионы.
Например: KOH = K+ + OH-
Ba(OH)2 = Ba2+ + 2OH-
3) Соли – это электролиты, которые диссоциируют на катионы металла и анионы кислотного остатка.
Например: Fe(NO3)3 = Fe3+ + 3NO3-
AlCl3 = Al3+ + 3Cl-
Похожие решебники
Популярные решебники 11 класс Все решебники
*К сожалению, временные проблемы с публикацией комментариев с мобильных устройств.









