Часть II Параграф 11 ГДЗ Рабочая тетрадь Габриелян 9 класс (Химия)
Решение #1


Рассмотрим вариант решения задания из учебника Габриелян, Сладков 9 класс, Дрофа:
Часть II
1. Запишите уравнения реакций, протекающих на воздухе с литием, лишённым вазелиновой защиты.
1) 4Li + O2 > 2Li2O
2) 6Li + N2 > 2Li3N
3) 2Li + 2H2O > 2LiOH + H2^
4) Li2O + CO2 > Li2CO3
Две первые реакции рассмотрите с позиций окислительно-восстановления (электронный баланс):
1) Li0 + O02 > Li+2O-2
O02 + 4e > 2O-2 4 4 1 – окислитель, восстановление
Li0 - e > Li+ 1 4 – восстановитель, окисление
4Li + O2 = 2Li2O
2) Li0 + N02 > Li+3N-3
N02 + 6e > 2N-3 6 6 1 – окислитель, восстановление
Li0 - e > Li+ 1 6 – восстановитель, окисление
6Li + N2 = 2Li3N
2. «По крыше выложили жесть» (В. В. Маяковский). Опишите процессы, происходящие с белой жестью при нарушении оловянной защиты: __________________.
Белая жесть – железный материал, изолированный от агрессивной среды слоем олова (луженое железо).
При нарушении защиты, оба металла, и железо, и олово одновременно окажутся в контакте с агрессивной средой. Поэтому более активное железо начнет коррозировать (выступать в качестве протектора олова).
3. Заполните таблицу «Свойства некоторых легированных сталей и их примесей».
ЛЕГИРУЮЩИЙ ЭЛЕМЕНТ — ОСОБЫЕ СВОЙСТВА СТАЛЕЙ — ПРИМЕНЕНИЕ
Легирующий элемент
Хром
Никель
Марганец
Титан
Вольфрам
Молибден
Ванадий
Особые свойства сталей
Повышенная прочность и химическая стойкость
Эластичность и пластичность
Повышенная прочность и химическая стойкость
Твердость и прочность
Твердость и жаропрочность
Эластичность и пластичность
Твердость и прочность
Применение
Детали приборов, части конструкций
Электроизмерительные приборы, монеты
Детали машин, электрические нагреватели
Промышленные установки
Детали машин,
Промышленные установки
Детали приборов
4. Опишите, какие способы защиты металлов от коррозии используются у вас в ванной комнате и на кухне: __________________.
Посуда из нержавеющей стали; хромированные краны и дверные ручки; эмалированные покрытия раковин.
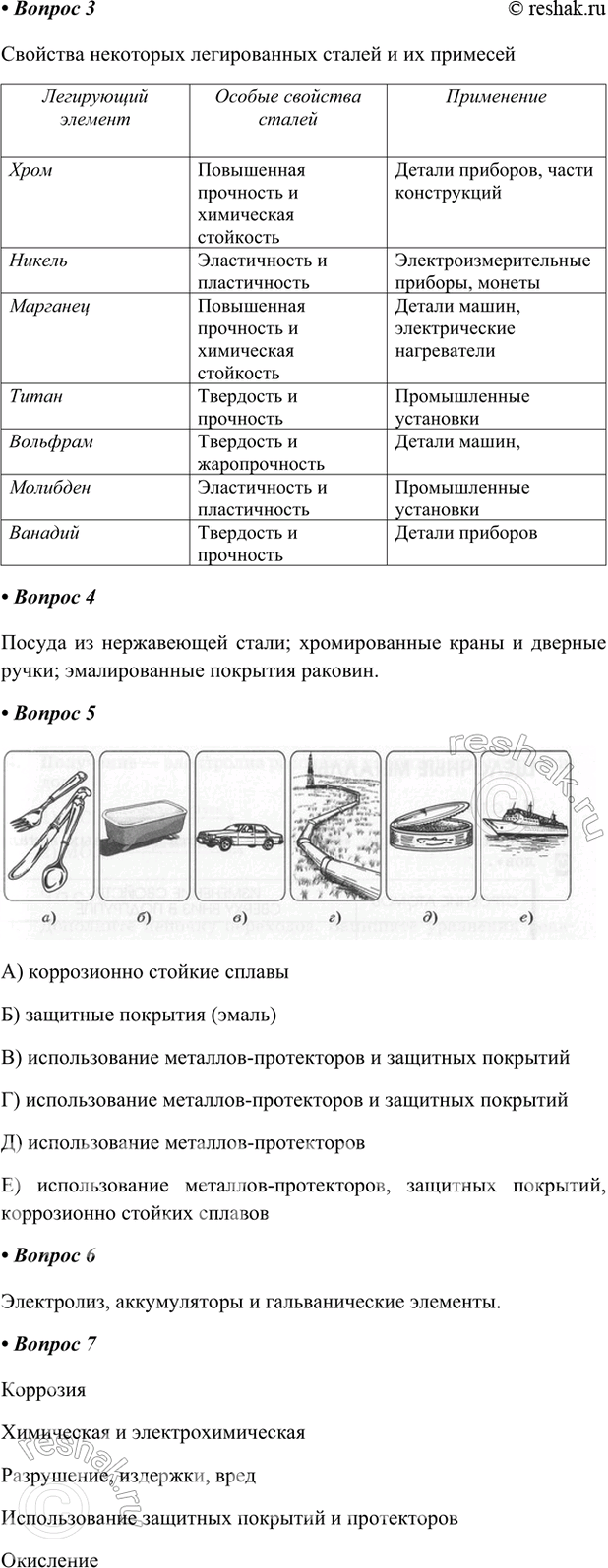
5. Перечислите наиболее часто используемые способы защиты от коррозии для изделий, изображённых на рисунках:
А) коррозионно стойкие сплавы
Б) защитные покрытия (эмаль)
В) использование металлов-протекторов и защитных покрытий
Г) использование металлов-протекторов и защитных покрытий
Д) использование металлов-протекторов
Е) использование металлов-протекторов, защитных покрытий, коррозионно стойких сплавов
6. Приведите примеры электрохимических процессов (электрохимической коррозии), приносящих людям пользу: __________________.
Электролиз, аккумуляторы и гальванические элементы.
7. Напишите синквейн о коррозии металлов: __________________.
Коррозия
Химическая и электрохимическая
Разрушение, издержки, вред
Использование защитных покрытий и протекторов
Окисление
Похожие решебники
Популярные решебники 9 класс Все решебники
*К сожалению, временные проблемы с публикацией комментариев с мобильных устройств.









