Часть ll Параграф 29 ГДЗ Рабочая тетрадь Габриелян Остроумов 9 класс (Химия)
Решение #1
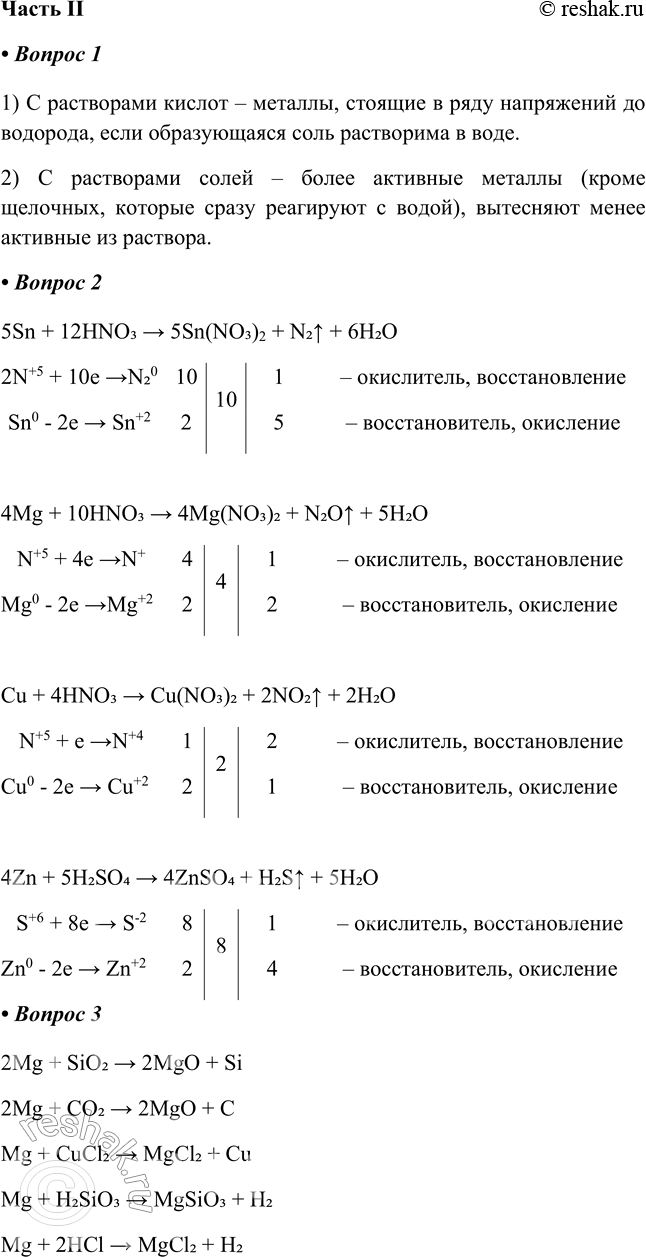

Рассмотрим вариант решения задания из учебника Габриелян, Остроумов, Сладков 9 класс, Просвещение:
Часть II
1. Сформулируйте два правила с указанием условий протекания реакций металлов в зависимости от их положения в ряду напряжений:
1) с растворами кислот:
2) с растворами солей:
1) С растворами кислот – металлы, стоящие в ряду напряжений до водорода, если образующаяся соль растворима в воде.
2) С растворами солей – более активные металлы (кроме щелочных, которые сразу реагируют с водой), вытесняют менее активные из раствора.
2. С помощью метода электронного баланса составьте уравнения реакций, соответствующих следующим схемам:
а) НNО3(разб.) + Sn - > Sn(NO3)2 + N2 +
б) НNО3(разб.) + Mg - > N2O +
в) HNO3(конц.) + Сu - >
г) H2SO4(конц.) + Zn — > H2S +
3. Запишите уравнения возможных реакций между магнием и следующими реагентами: оксид кремния(ІV), оксид кальция, оксид углерода(ІV), хлорид кальция, хлорид меди(ІІ), кремниевая
кислота, соляная кислота.
2Mg + SiO2 > 2MgO + Si
2Mg + CO2 > 2MgO + C
Mg + CuCl2 > MgCl2 + Cu
Mg + H2SiO3 > MgSiO3 + H2
Mg + 2HCl > MgCl2 + H2
4. В соляной кислоте растворили 36 г алюминиевой бронзы (сплав алюминия и меди). При этом выделилось 2,24 л водорода (н. у.). Определите массовую долю алюминия в исходном сплаве.
5. В концентрированной азотной кислоте растворили 208 г смеси меди и оксида меди(II). При этом выделилось 89,6 л оксида азота(ІV) (н. у.). Определите массовые доли компонентов исходной смеси и объём 60%-ной азотной кислоты (р — 1,20 г/мл), затраченной на реакцию.
Похожие решебники
Популярные решебники 9 класс Все решебники
*К сожалению, временные проблемы с публикацией комментариев с мобильных устройств.






