Часть l Параграф 24 ГДЗ Рабочая тетрадь Габриелян Остроумов 8 класс (Химия)
Решение #1

Рассмотрим вариант решения задания из учебника Габриелян, Остроумов, Сладков 8 класс, Просвещение:
§ 24. Основания, их классификация и свойства
Часть I
1. Основания — это
Основания – это сложные вещества, состоящие из атомов металла и одной или нескольких гидроксогрупп.
2. Оформите схему «Классификация оснований».
а) По числу гидроксогрупп, т. е. по
растворимые, или нерастворимые
Примеры
1) гидроксиды металлов ІА-группы
2) гидроксиды металлов IIА-группы
1) однокислотные
2) двухкислотные
3. Основания взаимодействуют:
1) с кислотами, образуя соль и воду
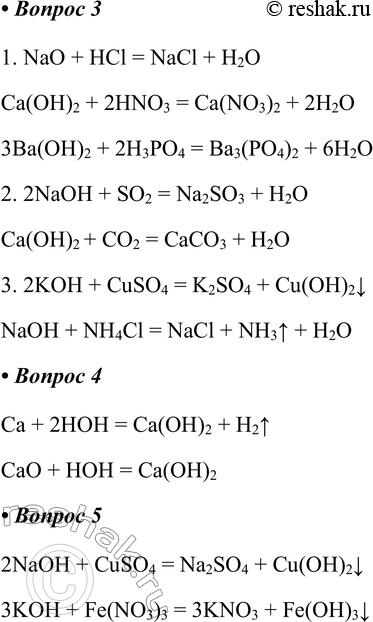
NaOH + НСl =________+________
Са(ОН)2 + HNO3 =________+________
Ва(ОН)2 + Н3РО4 =________+________
NaO + HCl = NaCl + H2O
Ca(OH)2 + 2HNO3 = Ca(NO3)2 + 2H2O
3Ba(OH)2 + 2H3PO4 = Ba3(PO4)2 + 6H2O
2) с кислотными оксидами, образуя соль и воду
NaOH + SO2 =________+________
Са(ОН)2 + СО2 =________+________
2NaOH + SO2 = Na2SO3 + H2O
Ca(OH)2 + CO2 = CaCO3 + H2O
3) с солями, если образуется ^ или v
КОН + CuSO4 =________+________
NaOH + NH4Cl =________+________
2KOH + CuSO4 = K2SO4 + Cu(OH)2v
NaOH + NH4Cl = NaCl + NH3^ + H2O
4. Щёлочи получают реакцией соединения и реакцией замещения соединений металлов ІА- и IIА-групп (начиная с Са) с водой:
Са + НОН =________+________
СаО + НОН =________
Ca + 2HOH = Ca(OH)2 + H2^
CaO + HOH = Ca(OH)2
5. Нерастворимые основания получают реакцией обмена между раствором щёлочи и солью металла нерастворимого гидроксида:
NaOH + CuSO4 =_________+_________
КОН + Fe(NO3)3 =_________+_________
2NaOH + CuSO4 = Na2SO4 + Cu(OH)2v
3KOH + Fe(NO3)3 = 3KNO3 + Fe(OH)3v
Похожие решебники
Популярные решебники 8 класс Все решебники
*К сожалению, временные проблемы с публикацией комментариев с мобильных устройств.








