Страница 190 ГДЗ Рабочая тетрадь Габриелян 8 класс (Химия)
Рассмотрим вариант решения задания из учебникаГабриелян 8 класс, Дрофа:
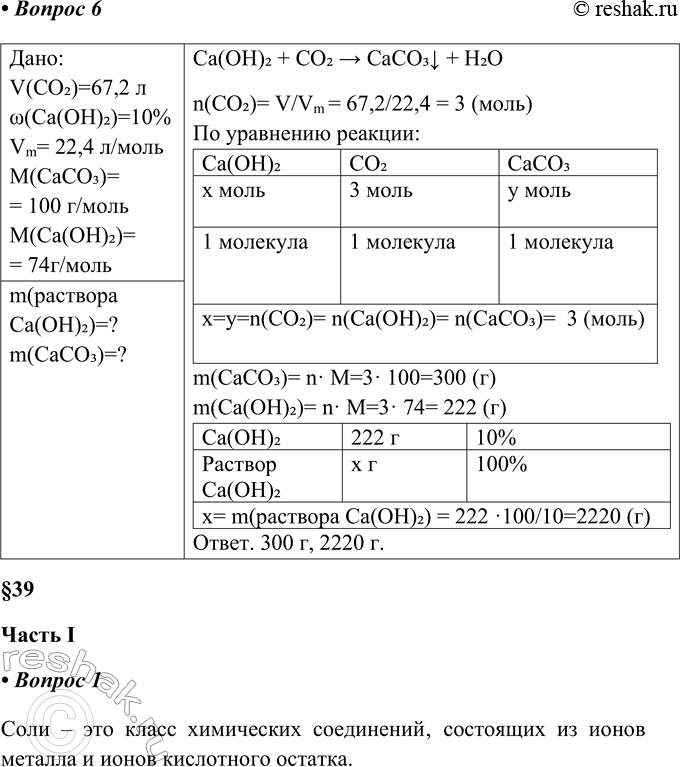
6. Вычислите массу (г) 10%-го раствора гидроксида кальция, необходимого для взаимодействия с 67,2 л углекислого газа (н, у.). Сколько граммов осадка образуется?
Дано:
V(CO2)=67,2 л
w(Ca(OH)2)=10%
Vm= 22,4 л/моль
M(CaCO3)= = 100 г/моль
M(Ca(OH)2)= = 74г/моль
m(раствора Ca(OH)2)=?
m(CaCO3)=?
Ca(OH)2 + CO2 > CaCO3v + H2O
n(CO2)= V/Vm = 67,2/22,4 = 3 (моль)
m(CaCO3)= n· M=3· 100=300 (г)
m(Ca(OH)2)= n· M=3· 74= 222 (г)
Ответ. 300 г, 2220 г.
СОЛИ, ИХ КЛАССИФИКАЦИЯ И ХИМИЧЕСКИЕ СВОЙСТВА В СВЕТЕ ТЭД
Часть I
1. Соли — это
Соли – это класс химических соединений‚ состоящих из ионов металла и ионов кислотного остатка.
Похожие решебники
Популярные решебники 8 класс Все решебники
*К сожалению, временные проблемы с публикацией комментариев с мобильных устройств.








