Практическая работа 1 ГДЗ Кузнецова Титова 9 класс (Химия)
Решение #1
Рассмотрим вариант решения задания из учебника Кузнецова, Титова, Гара 9 класс, Вентана-Граф:
Практическая работа 1
Влияние различных факторов на скорость химической реакции
Цель работы: изучить условия, влияющие на скорость протекания предложенных химических реакций; совершенствовать умения работать с химической посудой и реактивами.
Вспомните правила техники безопасности при работе с кислотами и нагревательными приборами.
Ход работы
1. Природа реагирующих веществ (состав и строение)
а) В две пробирки поместите немного чёрного порошка оксида меди (II). В первую пробирку добавьте 1 мл серной кислоты, а во вторую — 1 мл соляной кислоты. Наблюдайте признаки химической реакции. В какой из пробирок она протекает быстрее?
б) В одной пробирке смешайте твёрдые кристаллические соли: сульфат натрия и хлорид бария. В другой пробирке смешайте растворы этих солей. Отметьте свои наблюдения.
2. Площадь поверхности соприкосновения (контакта) веществ
а) В одну пробирку поместите железную кнопку или стружку, а в другую — порошок железа. Добавьте в каждую пробирку по 1 мл раствора сульфата меди (медного купороса). Через некоторое время наблюдайте произошедшие изменения.
б) В одну пробирку поместите кусочек мрамора, а в другую — мраморный порошок. Добавьте в каждую из пробирок по 1 мл соляной кислоты. Что наблюдаете?
3. Концентрация
В две пробирки поместите по одинаковому кусочку железной стружки или по одной грануле железа. В первую пробирку добавьте 1 мл разбавленной серной кислоты, а во вторую — 1 мл концентрированной серной кис лоты. В какой пробирке реакция протекает быстрее?
4. Температура
а) В пробирку поместите немного чёрного порошка оксида меди (II) и добавьте 1 мл разбавленной серной кислоты. Отметьте наблюдения. Затем пробирку немного нагрейте на пламени спиртовки (или в электронагревателе для пробирок). Что изменилось? Почему?
б) Получите гидроксид меди (II). Для этого в пробирку с 2 мл раствора сульфата меди добавьте (по каплям!) раствор щёлочи. Гидроксид меди (II) — студенистый осадок голубого цвета. Нагрейте его на пламени спиртовки (или в электронагревателе для пробирок). Отметьте признак реакции.
5. Катализатор
В пробирку налейте 2 мл перекиси водорода. Добавьте немного чёрного порошка оксида марганца (IV). Отметьте свои наблюдения.
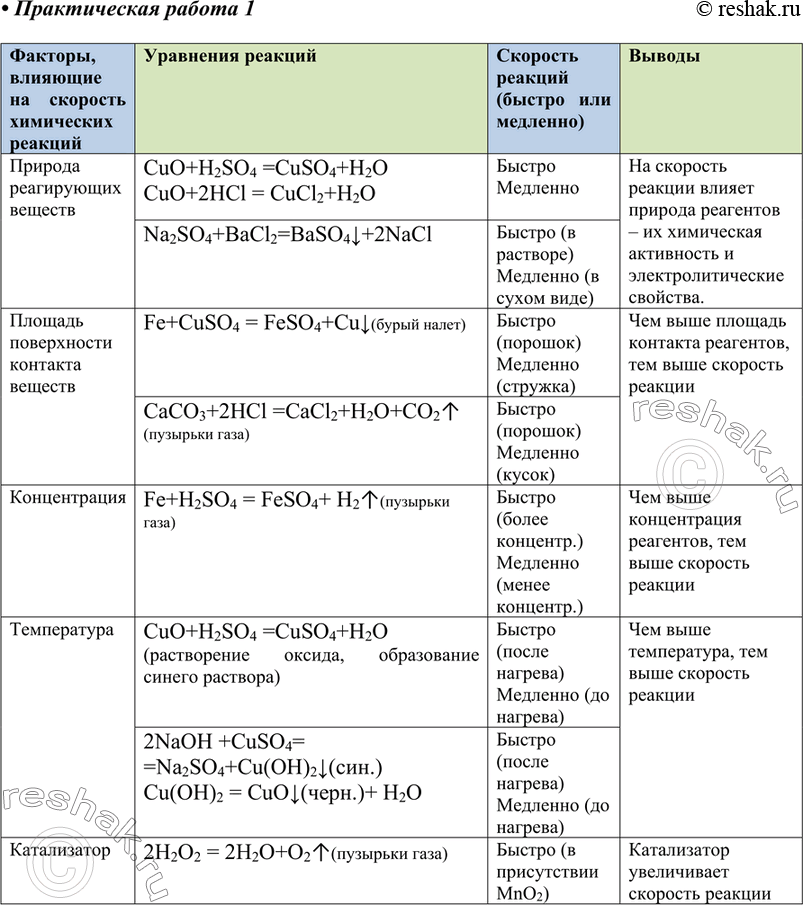
Отчёт о работе оформите в виде таблицы.
Популярные решебники 9 класс Все решебники
*К сожалению, временные проблемы с публикацией комментариев с мобильных устройств.





