Вопрос 4 Параграф 20 ГДЗ Рудзитис 9 класс (Химия)
Решение #1

Решение #2
Рассмотрим вариант решения задания из учебника Рудзитис, Фельдман 9 класс, Просвещение:
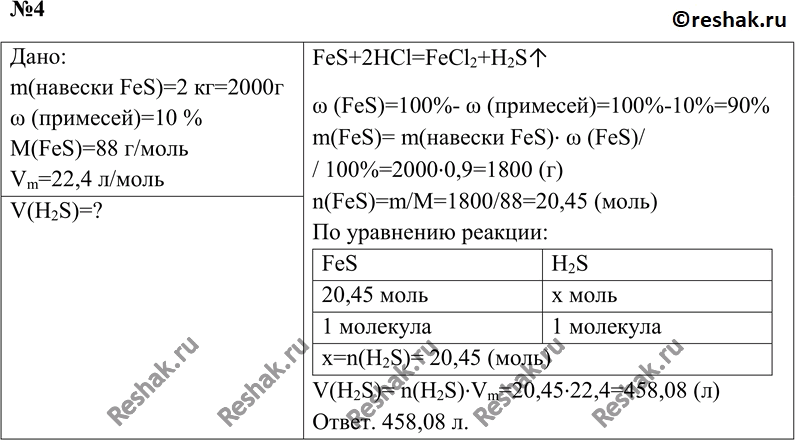
4. Определите объём сероводорода (н. у.), образовавшегося при реакции соляной кислоты с 2 кг сульфида железа(II), содержащего 10 % примесей.
FeS+2HCl=FeCl2+H2S^
? (FeS)=100%- ? (примесей)=100%-10%=90%
m(FeS)= m(навески FeS)· ? (FeS)/
/ 100%=2000·0,9=1800 (г)
n(FeS)=m/M=1800/88=20,45 (моль)
По уравнению реакции:
FeS H2S
20,45 моль x моль
1 молекула 1 молекула
x=n(H2S)= 20,45 (моль)
V(H2S)= n(H2S)·Vm=20,45·22,4=458,08 (л)
Ответ. 458,08 л.
Популярные решебники 9 класс Все решебники
*размещая тексты в комментариях ниже, вы автоматически соглашаетесь с пользовательским соглашением





