Готовимся к ЕГЭ Глава 4 ГДЗ Кузнецова Лёвкин 11 класс (Химия)
Решение #1




Рассмотрим вариант решения задания из учебника Кузнецова, Лёвкин, Шаталов 11 класс, Просвещение:
ГОТОВИМСЯ К ЕГЭ
1. Реакцией соединения является взаимодействие
1) натрия с водой
2) оксида натрия с водой
3) гидроксида натрия с сероводородом
4) натрия с водородом
5) алюминия с оксидом меди(II)
1) 2Na + 2H2O > 2NaOH + H2^
Это реакция замещения.
2) Na2O + H2O > 2NaOH
Это реакция соединения.
3) 2NaOH + H2S > Na2S + 2H2O
Это реакция обмена.
4) 2Na + H2 > 2NaH
Это реакция соединения.
5) 2Al + 3CuO > Al2O3 + 3Cu
Это реакция замещения.
Правильный ответ 24.
2. Экзотермической реакцией является
1) электролитическое разложение воды
2) термическое разложение карбоната кальция
3) горение этанола
4) дегидрирование этана
5) взаимодействие гидроксида натрия и соляной кислоты
Экзотермическими реакциями являются реакции горения и нейтрализации:
Горение этанола: C2H5OH + 3O2 > 2CO2^ + 3H2O + Q
Реакция нейтрализации: NaOH + HCl > NaCl + H2O + Q
Правильный ответ 35.
3. Каталитическими реакциями являются
1) синтез аммиака
2) нейтрализация гидроксида натрия уксусной кислотой
3) термическое разложение известняка
4) промышленное окисление оксида серы(ІV) до оксида серы(VІ)
5) взаимодействие натрия с водой
6) гидрирование бензола
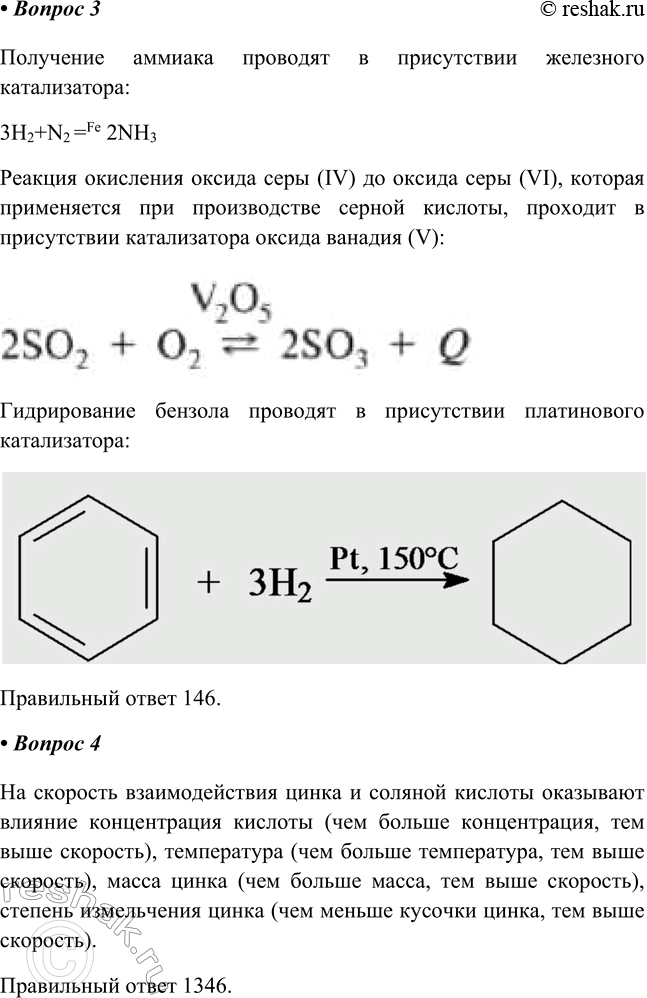
Получение аммиака проводят в присутствии железного катализатора:
3H2+N2 =Fe 2NH3
Реакция окисления оксида серы (IV) до оксида серы (VI), которая применяется при производстве серной кислоты, проходит в присутствии катализатора оксида ванадия (V)
Гидрирование бензола проводят в присутствии платинового катализатора
Правильный ответ 146.
4. На скорость взаимодействия цинка и соляной кислоты оказывают влияние
1) концентрация кислоты
2) объём выделяющегося водорода
3) температура
4) масса цинка
5) давление
6) степень измельчения цинка
На скорость взаимодействия цинка и соляной кислоты оказывают влияние концентрация кислоты (чем больше концентрация, тем выше скорость), температура (чем больше температура, тем выше скорость), масса цинка (чем больше масса, тем выше скорость), степень измельчения цинка (чем меньше кусочки цинка, тем выше скорость).
Правильный ответ 1346.
5. В реакции N2(r.) + О2(r.) 2NO(r.) — Q смещению равновесия в сторону образования оксида азота(ІІ) будет способствовать
1) понижение давления 2) повышение давления 3) нагревание системы 4) охлаждение системы 5) применение катализатора 6) повышение концентрации кислорода
N2 (г.) + O2 (г.) < - > 2NO (г.) – Q
2 молекулы газа превращаются в 2 молекулы газа, поэтому давление не оказывает влияние на смещение равновесия > ответы 1 и 2 неверные.
Катализатор не оказывает влияние на смещение равновесия > ответ 5 неверный.
Кислород – исходной вещество, поэтому увеличение его концентрации сместит равновесие в сторону образования продукта реакции. Ответ 6 верный.
Реакция эндотермическая, поэтому повышение температуры сместит равновесие вправо. Ответ 3 верный, ответ 4 неверный.
Правильный ответ 36.
6. Слабым электролитом является
1) фенол
2) азотистая кислота
3) ацетат аммония
4) хлорид аммония
5) раствор аммиака
6) фтороводородная кислота
7) сульфид натрия
К слабым электролитам относятся фенол, азотистая кислота, раствор аммиака и фтороводородная кислота.
7. Сокращённому ионному уравнению
Zn(OH)2 + 2Н+ = Zn2+ + 2Н2О
соответствует реакция
1) Zn(OH)2 + 2HNO3 = Zn(NO3)2 + 2Н2О
2) Zn(OH)2 + 2CH3COOH = (CH3COO)2Zn + 2H2O
3) Zn(OH)2 + H2SiO3, = ZnSiO3 + 2H2O
4) ZnO + H2SO4 = ZnSO4 + H2O
5) Zn(OH)2 + 2HBr = ZnBr2 + 2H2O
1) Zn(OH)2 + 2HNO3 = Zn(NO3)2 + 2H2O
Zn(OH)2 + 2H+ + 2NO3- > Zn2+ + 2NO3- + 2H2O
Zn(OH)2 + 2H+ = Zn2+ + 2H2O
5) Zn(OH)2 + 2HBr = ZnBr2 + 2H2O
Zn(OH)2 + 2H+ + 2Br- > Zn2+ + 2Br- + 2H2O
Zn(OH)2 + 2H+ = Zn2+ + 2H2O
Правильный ответ 15.
8. Установите соответствие между названием соли и отношением её к гидролизу (к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой).
Название соли Отношение к гидролизу
A) ацетат натрия Б) сульфат цезия B) бромид цинка Г) карбонад аммония 1) не гидролизуется 2) гидролизуется по катиону 3) гидролизуется по аниону 4) гидролизуется и по катиону, и по аниону
Соли, образованные сильными кислотами и сильными основаниями, не гидролизуются, сильными кислотами и слабыми основаниями – гидролизуются по катиону, слабыми кислотами и сильными основаниями – гидролизуются по аниону, слабыми кислотами и слабыми основаниями – гидролизуются по катиону и аниону
А Б В Г
3 1 2 4
9. Установите соответствие между названием соли и окраской лакмуса в её водном растворе (к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой).
Название соли Окраска лакмуса
А) нитрат алюминия 1) фиолетовая
Б) хлорид бария 2)синяя
В) сульфит калия 3) красная
Г) силикат натрия 4) оранжевая
Соли, образованные сильными кислотами и сильными основаниями, не гидролизуются (среда нейтральная, лакмус фиолетовый), сильными кислотами и слабыми основаниями – гидролизуются по катиону (среда кислая, лакмус красный), слабыми кислотами и сильными основаниями – гидролизуются по аниону (среда щелочная, лакмус синий)
А Б В Г
3 1 2 2
10. Установите соответствие между изменением степени окисления азота и схемой окислительно-восстановительной реакции (к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой).
А Б В Г
6 4 5 23
11. Установите соответствие между формулой вещества и продуктом (продуктами), образующимся на катоде при электролизе его водного раствора (к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой).
А Б В Г
1 5 5 5
12. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества (к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой).
Вещества Реактив
A) хлорид железа(ІII) и хлорид калия Б) сульфат аммония и сульфат калия B) соляная и азотная кислоты Г) нитрат цинка и нитрат магния 1) ВаСl2 2) AgNO3 3) Вr2(водн. р-р) 4) NaOH 5) фенолфталеин (р-р)
А) NaOH:
FeCl3 + 3NaOH > Fe(OH)3v (бурый осадок) + 3NaCl
KCl + 3NaOH > нет реакции
Б) NaOH:
(NH4)2SO4 + 2NaOH > 2NH3^ (запах аммиака) + Na2SO4 + 2H2O
K2SO4 + 3NaOH > нет реакции
В) AgNO3:
HCl + AgNO3 > AgClv + HNO3
HNO3 + AgNO3 > нет реакции
Г) NaOH (избыток):
Zn(NO3)2 + 4NaOH > Na2[Zn(OH)4] + 2NaNO3
Mg(NO3)2 + 2NaOH > Mg(OH)2v (белый осадок) + 2NaNO3
А Б В Г
4 4 2 4
Популярные решебники 11 класс Все решебники
*К сожалению, временные проблемы с публикацией комментариев с мобильных устройств.





