Практическая работа 2 ГДЗ Еремин Кузьменко 9 класс (Химия)
Решение #1


Рассмотрим вариант решения задания из учебника Еремин, Кузьменко 9 класс, Просвещение:
Практическая работа 2
Получение аммиака и изучение его свойств
Оборудование и реактивы: лабораторный штатив с лапкой, спиртовка, две сухие пробирки, газоотводная трубка с пробкой, ложечка, стеклянная палочка, вата, кристаллизатор с водой, штатив с пробирками, кусок фильтровальной бумаги, хлорид аммония, гидроксид кальция, раствор аммиака, раствор серной кислоты.
1. В небольшую фарфоровую чашку или на лист бумаги насыпьте две ложечки хлорида аммония и одну ложечку гидроксида кальция. Смесь перемешайте стеклянной палочкой (запах какого газа вы почувствовали?) и насыпьте в сухую пробирку.
В фарфоровой чашечке перемешивают стеклянной палочкой хлорид аммония и гидроксид кальция – появляется запах аммиака.
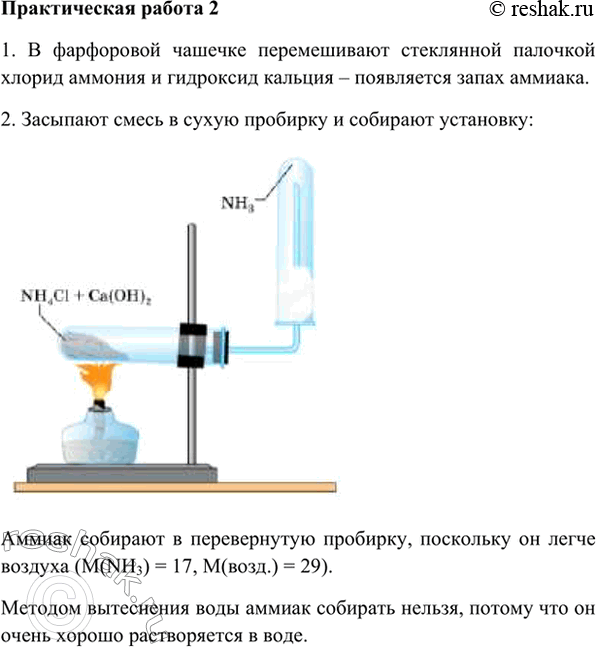
2. Укрепите пробирку со смесью в лапке штатива так, чтобы её дно находилось несколько выше её отверстия. В противном случае капли воды, образующейся в результате реакции, могут попасть на горячую часть пробирки, отчего она треснет. В отверстие пробирки поместите резиновую пробку с изогнутой стеклянной трубкой, которую направьте вверх (рис. 132). На неё повесьте другую пробирку, предназначенную для сбора аммиака. Обратите внимание, что эта пробирка, а также газоотводная трубка должны обязательно быть сухими. Отверстие перевёрнутой вверх дном пробирки закройте куском ваты. Объясните, почему аммиак собирают в пробирку, расположенную отверстием вниз. Можно ли собирать аммиак методом вытеснения воды? Почему?
Засыпают смесь в сухую пробирку и собирают установку:
Аммиак собирают в перевернутую пробирку, поскольку он легче воздуха (M(NH3) = 17, M(возд.) = 29).
Методом вытеснения воды аммиак собирать нельзя, потому что он очень хорошо растворяется в воде.
3. Слегка прогрейте пробирку пламенем спиртовки, а затем нагревайте в том месте, где находится смесь. Какое вещество образуется на стенках пробирки? Поднесите к отверстию пробирки для сбора газа кусочек фильтровальной бумаги, смоченной раствором фенолфталеина. Что наблюдаете? Повторяйте эту процедуру несколько раз до тех пор, пока не обнаружите аммиак. После этого прекратите нагревание. Напишите уравнение реакции.
При нагревании смеси на стенках пробирке начинает образовываться вода. Поскольку аммиак имеет щелочную среду, то посинение лакмусовой бумажки свидетельствует о том, что стал образовываться аммиак:
2NH4Cl + Ca(OH)2 = CaCl2 + 2H2O + 2NH3^
4. К отверстию пробирки с аммиаком поднесите стеклянную палочку, смоченную раствором соляной кислоты. Что происходит? Что представляет собой образовавшийся белый дым?
При внесении стеклянной палочки, смоченной соляной кислотой, в пробирку с аммиаком образуются белые пары хлорида аммония:
NH3 + HCl = NH4Cl
5. Налейте в пробирку 1—2 мл водного раствора аммиака, добавьте несколько капель фенолфталеина, а затем серной кислоты до исчезновения окраски. Напишите уравнение реакции.
В водном растворе аммиака щелочная среда, поэтому фенолфталеин окрашивается в малиновый цвет. При добавлении серной кислоты проходит реакция нейтрализации, поэтому фенолфталеин обесцвечивается:
2NH3 + H2SO4 = (NH4)2SO4
6. Сделайте выводы о физических и химических свойствах аммиака.
Таким образом, аммиак – бесцветный газ с характерным запахом, который хорошо растворяется в воде, а в химических реакциях проявляет основные свойства – дает в растворе щелочную среду и вступает с кислотами в реакции нейтрализации.
Популярные решебники 9 класс Все решебники
*К сожалению, временные проблемы с публикацией комментариев с мобильных устройств.





